GM501 GentleVit
GM501 GentleVit Freeze/GentleVit Thaw sont un ensemble de milieux prêts à l’emploi pour la vitrification et le réchauffement d’ovocytes et d’embryons humains.
Jusqu’à 5 cycles de vitrification (du même patient) peuvent être effectués avec une configuration de support. N’utilisez pas le même support pour différents patients!
Rev03_00
| Description | Nr. de Ref | Contenance |
|---|---|---|
| GM501 GentleVit Freeze Kit | 4 GVF_KIT1 | Matériel inclus dans le package: |
| 1 x 5 ml GentleVit Pre-vitrification Medium | ||
| 1 x 1 ml GentleVit Freeze Medium 1 | ||
| 1 x 1 ml GentleVit Freeze Medium 2 | ||
| 1 x 1 ml GentleVit Freeze Medium 3 | ||
| 1 x 1 ml GentleVit Freeze Medium 4 | ||
| 1 x 1,5 ml GentleVit Freeze Medium 5 | ||
| GM501 GentleVit Thaw Kit | 4 GVT_KIT1 | Matériel inclus dans le package: |
| 1 x 7,5 ml GentleVit Thaw Medium 1 | ||
| 1 x 1 ml GentleVit Thaw Medium 2 | ||
| 1 x 1 ml GentleVit Thaw Medium 3 | ||
| 1 x 1 ml GentleVit Thaw Medium 4 | ||
| 1 x 1 ml GentleVit Thaw Medium 5 | ||
| 1 x 1 ml GentleVit Thaw Medium 6 |
Données et informations sur le produit
- Composition:
- Spécifications du produit et contrôle qualité
- Vitrification d’ovocytes
- Vitrification d’embryons
- Précautions et mise en garde
- Instructions de conservation et stabilité
Composition:
- GM501 GentleVit Freeze/GentleVit Thaw sont des milieux à base d’HTF qui contiennent de l’HEPES, du saccharose, de l’albumine sérique humaine (12 à 20 g/litre). Le milieu de refroidissement contient également du DMSO, de l’éthylène glycol (EG) et du Ficoll.
- GM501 GentleVit Freeze/GentleVitThaw ne contiennent pas d’antibiotiques.
Spécifications du produit et contrôle qualité:
- Toutes les matières premières sont de la plus grande pureté disponible (en pharmacopée européenne et/ou aux normes USP), le cas échéant.
- Un certificat d’analyse est disponible pour chaque lot sur demande sur notre site Internet avec le numéro de lot correspondant.
- La fiche de données de sécurité de GM501 GentleVit Freeze/GentleVit Thaw sont disponible sur demande, et peut être téléchargée sur notre site Internet.
- GM501 GentleVit Freeze/GentleVit Thaw sont fabriquée et testée selon les spécifications suivantes :
pH: 7.20-7.50 (critère d’acceptation: 7.20-7.40)
Osmolalité (mOsm/kg):
- 270-295 (GPI/GT6: critère d’acceptation: 270-290)
- 805-865 (GT3: critère d’acceptation: 805-850)
- 535-565 (GT4)
- 405-435 (GT5)
Stérilité: stérile – niveau d’assurance de stérilité (SAL) 10-3
Endotoxines (EU/ml): < 0.25
MEA: ≥80 (Test sur embryons de souris à 1 cellule, blastocystes après 96 h en %)
Vitrification d’ovocytes:
Préparation pour la vitrification:
- S’assurer que toutes les bouteilles de milieu du kit sont bien mélangées avant utilisation et réchauffées à température ambiante (20-25°C). Nous recommandons fortement la lecture de toutes les étapes de la procédure de vitrification/réchauffement avant de commencer la procédure.
Étapes préliminaires:
- Dans une boîte 6 puits, remplir le premier puits avec 250-300 µl de milieu GentleVit Pre-vitrification, le deuxième de Freeze Medium 1 et le troisième de Freeze Medium 2 et continuer de la sorte jusqu’au milieu Freeze Medium 5.
- Ouvrir le nombre nécessaire de dispositifs de vitrification, en prenant en compte qu’un dispositif peut contenir 2 à 3 ovocytes, dans une charge de volume maximale de 1 µl (vérifier les instructions pour le dispositif que vous utilisez). Placer les différentes parties du dispositif de façon pratique sur la paillasse pour qu’elles soient facilement accessibles plus tard dans la procédure.
Protocole de vitrification:
- Les ovocytes sont successivement exposés aux milieux suivants:
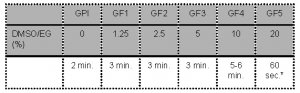
*Remarque: Le processus complet de dépôt de l’ovocyte dans le milieu « Freeze Medium 5 », de chargement de l’ovocyte sur le dispositif de vitrification dans un volume maximal de 1 µl de GF5, d’insertion du dispositif dans la paillette externe et de scellement ne devrait pas prendre plus de 60 secondes avant de plonger le dispositif dans l’azote liquide.
Décongélation d’ovocytes:
Préparation pour la décongélation:
- S’assurer que toutes les bouteilles de milieu du kit sont bien mélangées avant utilisation et réchauffées à température ambiante (20-25°C). Une exception est le milieu Warming 1 qui doit être réchauffé jusqu’à 37°C avant utilisation. Nous recommandons fortement la lecture de toutes les étapes de la procédure de vitrification/réchauffement avant de commencer la procédure.
Étapes préliminaires:
- Procédure de décongélation : Dans une boîte 6 puits, remplir le premier puits avec 500-800 µl de milieu Thaw Medium 1, le deuxième de Thaw Medium 2 et le troisième de Thaw Medium 3 et continuer de la sorte jusqu’au milieu Thaw Medium 6.
Protocole de décongélation:
- Dans la première étappe, tournoyer la paille dans GT1 (assurer une température plus homogène).
- Les ovocytes sont successivement exposés aux milieux suivants:
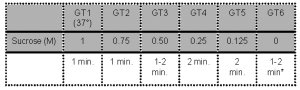
*Remarque: Laver pendant 1 à 2 minutes avant de transférer dans le milieu de culture.
Vitrification d’embryons (du stade zygote jusqu’au stade blastocyste):
Préparation pour la vitrification:
- S’assurer que toutes les bouteilles de milieu du kit sont bien mélangées avant utilisation et réchauffées à température ambiante (20-25°C). Nous recommandons fortement la lecture de toutes les étapes de la procédure de vitrification/réchauffement avant de commencer la procédure.
Étapes préliminaires:
- Pour la vitrification d’embryons, les milieux suivants NE sont PAS requis:
GentleVit Freeze Medium 1
GentleVit Freeze Medium 2
- Dans une boîte 6 puits, remplir le premier puits avec 250-300 µl de milieu GentleVit Pre-vitrification, le deuxième de Freeze Medium 3, le troisième de Freeze Medium 4 et le dernier de Freeze Medium 5.
- Ouvrir le nombre nécessaire de dispositifs de vitrification, en prenant en compte qu’un dispositif peut contenir 1 à 2 embryons, dans une charge de volume maximale de 1 µl (vérifier les instructions pour le dispositif que vous utilisez). Placer les différentes parties du dispositif de façon pratique sur la paillasse pour qu’elles soient facilement accessibles plus tard dans la procédure.
Protocole de vitrification:
- Les embryons sont successivement exposés aux milieux suivants:
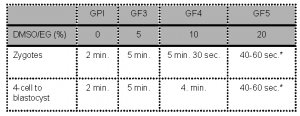
*Remarque: Le processus complet de dépôt de l’ovocyte dans le milieu « Freeze Medium 5 », de chargement de l’ovocyte sur le dispositif de vitrification dans un volume maximal de 1 µl de GF5, d’insertion du dispositif dans la paillette externe et de scellement ne devrait pas prendre plus de 60 secondes avant de plonger le dispositif dans l’azote liquide.
Décongélation d’embryons (du stade zygote jusqu’au stade blastocyste):
Préparation pour la décongélation:
- S’assurer que toutes les bouteilles de milieu du kit sont bien mélangées avant utilisation et réchauffées à température ambiante (20-25°C). Une exception est le milieu Warming 1 qui doit être réchauffé jusqu’à 37°C avant utilisation. Nous recommandons fortement la lecture de toutes les étapes de la procédure de vitrification/réchauffement avant de commencer la procédure.
Étapes préliminaires:
- Pour la décongélation d’embryons du stade 4 cellules au stade blastocyste, les milieux suivants NE sont PAS requis :
GM501 GentleVit Thaw Medium 5
- Dans une boîte 6 puits, remplir le premier puits avec 500-800
- µl de milieu Thaw Medium 1, le deuxième de Thaw Medium 2 et le troisième de Thaw Medium 3, le quatrième de Thaw Medium 4, le cinquième de Thaw Medium 5 (uniquement pour les zygotes) et le dernier de Thaw Medium 6.
Protocole de décongélation:
- Dans la première étappe, tournoyer la paille dans GT1 (assurer une température plus homogène).
- Les embryons sont successivement exposés aux milieux suivants:
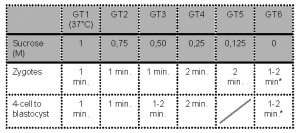
* Remarque: Laver pendant 1 à 2 minutes avant de transférer dans le milieu de culture.
Précautions et mise en garde:
- Les mesures standard de prévention des infections résultant de l’utilisation de produits de santé préparés à partir de sang ou de plasma humains comprennent la sélection des donneurs, le dépistage des dons individuels et des mélanges de plasma pour des marqueurs spécifiques d’infection et l’inclusion d’étapes de fabrication efficaces pour l’inactivation/élimination des virus. Malgré cela, lorsque des produits de santé préparés à partir de sang ou de plasma humains sont administrés, la possibilité d’une transmission d’agents infectieux ne peut pas être complètement exclue. Ceci s’applique aussi aux virus inconnus ou émergents et autres pathogènes. Aucune transmission avérée de virus n’a été rapportée avec l’albumine fabriquée selon les spécifications de la pharmacopée européenne par les processus établis.
- Par conséquent, manipuler tous les échantillons comme s’ils pouvaient transmettre le VIH ou l’hépatite. Toujours porter des vêtements de protection lors de la manipulation d’échantillons.
- Toujours travailler dans des conditions d‘hygiène rigoureuses (hotte à flux laminaire ISO 5) pour éviter une contamination potentielle.
À n’utiliser que pour l’usage prévu. - La sécurité à long terme de la vitrification des embryons et oocyte sur les enfants nés à la suite de cette procédure est inconnue.
- L’établissement de l’utilisateur de ce dispositif est responsable de la maintenance de la traçabilité du produit et doit respecter les réglementations nationales concernant la traçabilité, s’il y a lieu.
Vérifications avant utilisation:
- Ne pas utiliser le produit si la bouteille, l’opercule du conteneur ou l’emballage est ouvert ou défectueux à la livraison du produit.
- Ne pas utiliser le produit s’il est décoloré, trouble ou présente le moindre signe de contamination microbienne.
Instructions de conservation et stabilité:
- La durée de conservation est de 12 mois à partir du moment de la fabrication.
- Conserver entre 2 et 8°C.
- Ne pas congeler avant utilisation.
- Conserver à l‘abri de la lumière (du soleil).
- Le produit peut être utilisé sans problème jusqu’à 7 jours après ouverture, lorsque des conditions stériles sont maintenues et que les produits sont conservés à 2-8°C.
- Stable après transport (5 jours maximum) à température élevée (£ 37°C).
- Le contenu ne peut pas être stérilisé à nouveau après ouverture.
- Ne pas utiliser après la date d’expiration.

